Informes de efectos adversos graves y fallecimientos para las principales vacunas COVID, según el VAERS
Nefropatía membranosa tras la vacunación por COVID-19
13 diciembre, 2022
Sam Bankman-Fried de FTX es arrestado en las Bahamas
13 diciembre, 2022Hasta el 2 de diciembre de 2022 se habían notificado un total de 906,544 efectos adversos relacionados con todas las vacunas contra el COVID-19 aprobadas en Estados Unidos, incluidos 15,584 fallecimientos, según el Sistema para Reportar Eventos Adversos a las Vacunas (VAERS, por sus siglas en inglés).
Estas vacunas contra el COVID-19 han dado lugar a más notificaciones de acontecimientos adversos en el sistema VAERS que todas las notificaciones realizadas en las últimas tres décadas. En concreto, el número de muertes relacionadas con la vacuna contra el COVID-19 ha superado el 55% de todas las notificaciones de muertes por vacunas en VAERS.
Desgraciadamente, debido a diversos problemas las cifras reales de los distintos acontecimientos adversos pueden superar con creces las cifras que aparecen en el sistema VAERS.
Cualquiera puede enviar un reporte al sistema VAERS
Iniciado en 1990, el sistema VAERS es una consecuencia de la Ley Nacional de Lesiones Causadas por Vacunas Infantiles (NCVIA) de 1986. Como sistema de vigilancia y alerta temprana de la seguridad de las vacunas en Estados Unidos, el VAERS está gestionado conjuntamente por los Centros para el Control y la Prevención de Enfermedades (CDC, por sus siglas en inglés) y la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés).
Dado que los informes del VAERS proporcionan a las autoridades sanitarias estadounidenses información importante sobre problemas de salud relacionados con las vacunas, los CDC y la FDA supervisan el sistema con regularidad, y analizan e investigan casos concretos para tomar las medidas necesarias, en su caso.
Cualquier persona, como receptores de vacunas, padres/tutores de receptores de vacunas, profesionales médicos, fabricantes de vacunas y la república en general, puede enviar un informe sobre acontecimientos adversos de vacunas al sistema VAERS, ya sean leves o graves. Sin embargo, VAERS no puede demostrar la causalidad entre una vacuna y un acontecimiento adverso.
Los efectos adversos graves de las vacunas pueden incluir visitas a urgencias, muertes, efectos secundarios potencialmente mortales, discapacidad permanente, malformaciones congénitas y hospitalizaciones. Y a efectos de este artículo, todos estos efectos adversos se examinan en relación con vacunas específicas.
Limitaciones del VAERS
El sistema VAERS tiene sus limitaciones, incluido el grave problema de los registros menores que las cifras reales. Según el estudio Harvard Pilgrim Health Care realizado entre 2005 y 2009, tras la administración de 1.4 millones de vacunas, solo se habían notificado al sistema VAERS menos del 1% de los acontecimientos adversos. Además, varios analistas independientes han estimado que solo el 2.5 por ciento de las reacciones adversas a las vacunas contra el COVID se notifican al VAERS.
Otro problema que ha venido aquejando al sistema de notificación es su redundancia. En concreto, un acontecimiento adverso puede tener diferentes nombres. Por ejemplo, el dolor en el lugar de la inyección y el dolor en el lugar de la vacuna se introducen en el sistema como síntomas separados; y una persona que notifica el problema puede seleccionar ambos síntomas.
Además, un estudio publicado en la revista Vaccine descubrió que es más probable que las personas notifiquen acontecimientos adversos más graves.
Además, según un estudio revisado por pares publicado en octubre de 2021 por la bióloga molecular canadiense Jessica Rose en relación con el sistema VAERS, debido a las constantes actualizaciones y a que algunos datos no se introducen a tiempo, el sistema tiene un problema de acumulación de datos.
El estudio de Rose también descubrió un problema más preocupante. Es decir, algunos informes adversos por la vacuna contra el COVID-19 habían sido eliminados del sistema VAERS sin explicación, incluidos 1516 informes eliminados entre el 17 de diciembre de 2020 y el 6 de agosto de 2021. En octubre de 2021, cuando se publicó su estudio, el número de informes VAERS eliminados sobre vacunas contra el COVID-19 representaba el 0.4 por ciento de todos los eventos adversos de VAERS, según lo identificado por sus ID de VAERS.
Actualmente, existen cuatro vacunas contra el COVID-19 para series primarias, y otras dos vacunas bivalentes utilizadas como refuerzos.
Vacuna contra el COVID-19 de Pfizer-BioNTech
Comercializada bajo la marca Comirnaty, la vacuna contra el COVID-19 de Pfizer-BioNTech es producida por la empresa alemana BioNTech.
El 11 de diciembre de 2020, la FDA emitió una autorización de uso de emergencia (EUA) para la vacuna. Al día siguiente, los CDC recomendaron el uso de la vacuna a partir de los 16 años.
El 23 de agosto de 2021, la FDA aprobó el uso de la vacuna Pfizer-BioNTech contra el COVID-19 en personas de 16 años o más. Así, la vacuna de Pfizer-BioNTech se convirtió en la primera vacuna contra el COVID-19 aprobada por la FDA. Posteriormente, la FDA modificó la EUA emitida para la vacuna, con el fin de ampliar la población aprobada para recibir esta vacuna para incluir a niños mayores de 6 meses.
El 31 de agosto de 2022, la FDA modificó la EUA de la vacuna contra el COVID-19 de Pfizer-BioNTech para autorizar su vacuna bivalente (es decir, el “refuerzo actualizado”) para su uso como dosis única de refuerzo.
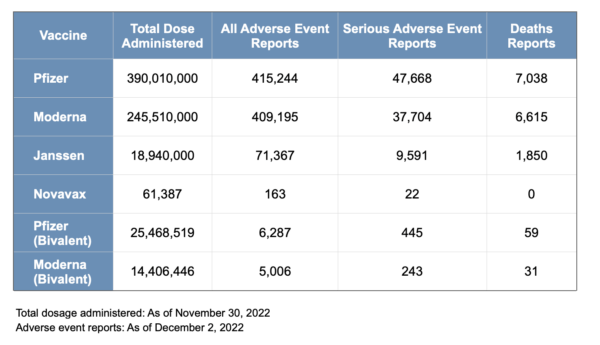
Cifras de informes de acontecimientos adversos del VAERS: Según VAERS, hasta el 2 de diciembre de 2022, se habían notificado un total de 415,244 acontecimientos adversos relacionados con la vacuna monovalente contra el COVID-19 de Pfizer-BioNTech, incluidos 47,668 acontecimientos adversos graves y 7038 fallecimientos (que forman parte de los acontecimientos adversos graves).
Cantidad de vacunas administradas: Según Our World in Data, hasta el 30 de noviembre de 2022 se habían administrado 390,01 millones de dosis de la vacuna contra el COVID-19 de Pfizer-BioNTech en Estados Unidos, lo que la convierte en la vacuna contra el COVID-19 más utilizada en el país.
Dosis aprobadas actualmente: En cuanto a la vacuna monovalente Pfizer-BioNTech, la dosis actualmente aprobada es de dos dosis para su serie primaria. Los CDC también recomiendan el uso de la vacuna como dosis de refuerzo para las personas que hayan completado su serie primaria. Si alguien recibe una dosis de refuerzo, es su tercera dosis en total; si recibe una segunda dosis de refuerzo, entonces es su cuarta dosis.
La vacuna bivalente contra el COVID-19 de Pfizer-BioNTech fue recomendada posteriormente por los CDC para su uso como dosis de refuerzo actualizada.
Vacuna contra COVID-19 de Moderna
Comercializada bajo la marca Spikevax, la vacuna contra COVID-19 de Moderna es producida por la empresa estadounidense Moderna. El 18 de diciembre de 2020, la FDA emitió una EUA para el uso de la vacuna en personas mayores de 18 años.
El 31 de enero de 2022, la FDA aprobó el uso de la vacuna contra el COVID-19 de Moderna en personas mayores de 18 años. Posteriormente, la FDA modificó la EUA emitida para la vacuna, para ampliar la población aprobada para recibir esta vacuna para incluir a niños mayores de 6 meses.
El 31 de agosto de 2022, la FDA modificó la EUA de la vacuna de Moderna para autorizar su vacuna bivalente para su uso como dosis de refuerzo.
Cifras de informes de acontecimientos adversos del VAERS: Según VAERS, hasta el 2 de diciembre de 2022, se habían notificado un total de 409,195 acontecimientos adversos relacionados con la vacuna monovalente contra COVID-19 de Moderna, incluidos 37,704 acontecimientos adversos graves y 6615 fallecimientos.
Cantidad de vacunas administradas: Según Our World in Data, hasta el 30 de noviembre de 2022, se habían administrado 245.51 millones de dosis de la vacuna contra COVID-19 de Moderna en Estados Unidos.
Dosis aprobadas actualmente: En cuanto a la vacuna monovalente contra el COVID-19 Moderna, la dosis actualmente aprobada es de dos dosis para su serie primaria. Los CDC también recomiendan el uso de la vacuna como dosis de refuerzo para las personas que hayan completado su serie primaria. Si alguien recibe una dosis de refuerzo, es su tercera dosis en total; si recibe una segunda dosis de refuerzo, entonces es su cuarta dosis.
Los CDC recomiendan el uso de la vacuna bivalente contra COVID-19 de Moderna como dosis de refuerzo actualizada.
Vacuna contra COVID-19 de Johnson & Johnson (Janssen)
Introducida a principios de 2021, la vacuna contra el COVID-19 de Janssen es producida por una filial de Johnson & Johnson. El 27 de febrero de 2021, la FDA emitió una EUA para el uso de la vacuna en personas mayores de 18 años. Posteriormente, debido a los casos notificados de trombosis con síndrome de trombocitopenia y síndrome de Guillain-Barré después de recibir la vacuna, el 5 de mayo de 2022, la FDA limitó el uso de esta vacuna a adultos mayores de 18 años, para los que otras vacunas contra COVID-19 autorizadas no están disponibles o son clínicamente inapropiadas.
Cifras de informes de eventos adversos del VAERS: Según VAERS, hasta el 2 de diciembre de 2022, se habían notificado un total de 71,367 acontecimientos adversos relacionados con la vacuna contra COVID-19 de Janssen, incluidos 9591 acontecimientos adversos graves y 1850 fallecimientos.
Cantidad de vacunas administradas: Según Our World in Data, hasta el 30 de noviembre de 2022, se habían administrado 18.94 millones de dosis de la vacuna contra COVID-19 de Janssen en Estados Unidos.
Dosis aprobada actualmente: La FDA recomienda una única dosis de vacuna primaria para la vacuna contra el COVID-19 de Janssen, y los CDC también recomiendan una única dosis de refuerzo para esta vacuna, que debe tener lugar al menos dos meses después de la dosis primaria.
Vacuna contra el COVID-19 de Novavax
La vacuna contra el COVID-19 de Nuvaxovid es fabricada por la empresa estadounidense Novavax, Inc. El 19 de octubre de 2022, la empresa recibió una EUA emitida por la FDA para el uso de su vacuna contra la infección por COVID-19. La vacuna se utiliza como serie primaria entre personas de 12 años o más.
Cifras de informes de eventos adversos del VAERS: Según VAERS, hasta el 2 de diciembre de 2022, se habían notificado un total de 163 acontecimientos adversos relacionados con la vacuna contra el COVID-19 de Novavax, incluidos 22 acontecimientos adversos graves pero ninguna muerte.
Cantidad de vacunas administradas: Según Our World in Data, hasta el 30 de noviembre de 2022, se habían administrado 61,387 dosis de la vacuna contra el COVID-19 de Novavax en Estados Unidos.
Dosis aprobadas actualmente: La FDA recomienda dos dosis de vacuna primaria para la vacuna contra el COVID-19 de Novavax. Y según una recomendación de los CDC, una vez completada la serie primaria, se puede utilizar otra dosis de la vacuna Novavax como vacuna de refuerzo, y debe administrarse con un intervalo de tres a ocho semanas desde la última dosis.
Vacuna bivalente contra COVID-19 de Pfizer-BioNTech
El 31 de agosto de 2022, la FDA modificó la EUA de la vacuna contra el COVID-19 de Pfizer-BioNTech para autorizar su formulación bivalente como dosis de refuerzo. Esta vacuna bivalente está dirigida contra la variante original de Wuhan del virus SARS-CoV-2 y la variante ómicron.
El 8 de diciembre de 2022, la FDA modificó la EUA de la vacuna bivalente contra el COVID-19 de Pfizer-BioNTech para incluir su uso en niños a partir de 6 meses de edad.
Cifras de informes de acontecimientos adversos del VAERS: Según VAERS, hasta el 2 de diciembre de 2022, se habían notificado un total de 6287 acontecimientos adversos relacionados con la vacuna bivalente contra el COVID-19 de Pfizer-BioNTech, incluidos 445 acontecimientos adversos graves y 59 fallecimientos.
Cantidad de vacunas administradas: Según los CDC, hasta el 30 de noviembre de 2022, se habían administrado 25,468,519 dosis de la vacuna bivalente contra el COVID-19 de Pfizer-BioNTech en Estados Unidos.
Dosis aprobada actualmente: Las personas deben recibir este “refuerzo actualizado” al menos dos meses después de la serie primaria o de la última vacunación de refuerzo.
Vacuna bivalente contra COVID-19 de Moderna
El 31 de agosto de 2022, la FDA modificó la EUA de la vacuna contra COVID-19 de Moderna para autorizar su formulación bivalente para su uso como dosis única de refuerzo. Esta vacuna bivalente también está dirigida contra la variante original del virus SARS-CoV-2, así como contra la variante ómicron.
El 8 de diciembre de 2022, la FDA modificó la EUA de la vacuna bivalente contra el COVID-19 de Moderna para incluir su uso en niños a partir de 6 meses de edad.
Cifras de informes de acontecimientos adversos del VAERS: Según VAERS, hasta el 2 de diciembre de 2022, se habían notificado un total de 5006 acontecimientos adversos relacionados con la vacuna bivalente contra el COVID-19 de Moderna, incluidos 243 acontecimientos adversos graves y 31 fallecimientos.
Cantidad de vacunas administradas: Según los CDC, hasta el 30 de noviembre de 2022 se habían administrado 14,406,446 dosis de la vacuna bivalente contra el COVID-19 de Moderna en Estados Unidos.
Dosis aprobada actualmente: Se recomienda utilizar la vacuna bivalente contra el COVID-19 de Moderna como dosis de refuerzo.
Efectos adversos desconocidos de la vacuna notificados en VAERS
Según el VAERS, hasta el 2 de diciembre de 2022, se habían notificado un total de 4677 acontecimientos adversos relacionados con vacunas desconocidas, incluidos 629 acontecimientos adversos graves y 61 muertes.
En total, se han notificado 906,544 efectos adversos relacionados con todas las vacunas contra el COVID-19 aprobadas en Estados Unidos, incluidos 95,695 efectos adversos graves y 15,584 fallecimientos.
Te recomendamos éste PodCast donde se habla de éste tema.
Únete a nuestra comunidad de Telegram comenta, opina, comparte.




